Leki a zespół suchego oka – przegląd informacji
Udostępnij
Zespół suchego oka (ZSO) jest chorobą charakteryzującą się utratą homeostazy filmu łzowego. ZSO nie tylko prowadzi do pogorszenia jakości życia z powodu dolegliwości, takich jak uczucie ciała obcego pod powiekami, pieczenia i swędzenia, ale także do obniżenia ostrości wzroku i erozji nabłonka rogówki. Wiele spośród powszechnie stosowanych leków wpływa na pracę gruczołów związanych w tworzeniem filmu łzowego, zaburzając jego homeostazę.
Zespół suchego oka – ZSO (DSE, ang. Dry-Eye Syndrome), chociaż wydaje się być niegroźną przypadłością, powoduje pogorszenie jakości życia w stopniu porównywalnym na przykład z łuszczycą [1].
ZSO jest wieloczynnikową chorobą powierzchni oka, charakteryzującą się utratą homeostazy filmu łzowego, w której rolę etiologiczną odgrywają: niestabilność i hiperosmolarność filmu łzowego, zapalenie i uszkodzenie powierzchni oka oraz zaburzenia neurosensoryczne [2].
ZSO może prowadzić do erozji nabłonka rogówki, co szczególnie dotkliwie odczuwają użytkownicy soczewek kontaktowych. Wystąpienie ZSO wiąże się z nieprawidłowym funkcjonowaniem tzw. filmu łzowego.
|
Choroby systemowe, z którymi zwykle związane jest występowanie ZSO [28]: |
|
Film łzowy jest cienką powłoką pokrywającą powierzchnię gałki ocznej, biorącą udział w jej ochronie (zarówno przed uszkodzeniami mechanicznymi, jak i drobnoustrojami), dostarczającą rogówce substancji odżywczych i zapewniającą jej powierzchni gładkość. Film łzowy jest zbudowany z trzech warstw.
Od zewnątrz, od strony powietrza, znajduje się warstwa lipidowa, spowalniająca parowanie znajdującej się pod nią warstwy wodnej. Najbliżej powierzchni gałki ocznej znajduje się natomiast warstwa śluzowa (mucynowa), wydzielana przez komórki kubkowe spojówki, która zapewnia filmowi łzowemu odpowiednie przyleganie i stabilność na powierzchni oka [3].
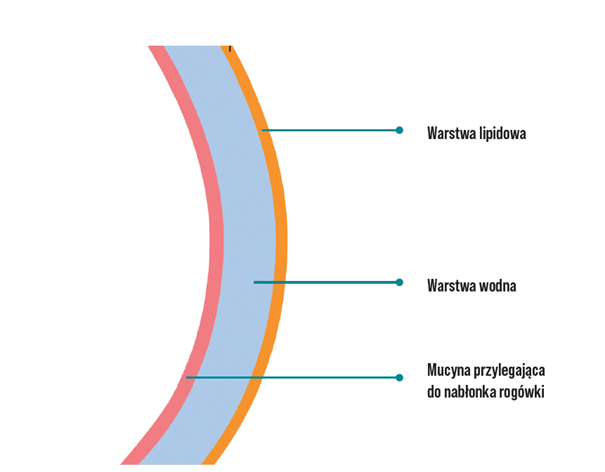
Rycina 1. Model trójwarstwowy struktury filmu łzowego [29]
Film łzowy jest formowany na nowo po każdym mrugnięciu. Kilkanaście sekund po uformowaniu traci on swoją stabilność, głównie na skutek parowania składowej wodnej, aż w końcu dochodzi do przerwania jego ciągłości.
Prawidłowa, trójwarstwowa struktura pozwala na wystarczająco długie utrzymanie się filmu łzowego na powierzchni oka i właściwe pełnienie przez niego swoich funkcji.
Jednak wiele spośród stosowanych powszechnie leków może prowadzić do zaburzeń wydzielania przez gruczoły poszczególnych składowych filmu łzowego, prowadząc do skrócenia jego czasu przerwania (TBUT, ang. tear film break up time) do wartości krótszej niż czas pomiędzy poszczególnymi mrugnięciami.
|
Czynniki zwiększające prawdopodobieństwo wystąpienia ZSO [28]: |
|
Diagnostyka i objawy
Diagnostyka ZSO opiera się na stwierdzeniu obecności objawów, takich jak uczucie pieczenia, kłucia lub swędzenia oczu, uczucie ciała obcego, obecność wydzieliny na brzegach powiek, zaczerwienienia oczu i nadwrażliwości na światło.
Ponadto kluczowymi badaniami w diagnostyce ZSO jest czas przerwania filmu łzowego, wynik testu Schirmera oraz badanie w lampie szczelinowej, zwłaszcza podczas tak zwanej próby fluoresceinowej, czyli oceny wybarwienia rogówki, spojówki i brzegów powiek po zaaplikowaniu barwnika fluoresceiny.
Poza tymi parametrami coraz istotniejszą rolę odgrywa oznaczanie osmolarności składowej wodnej (w ZSO film łzowy charakteryzuje się większym zasoleniem), interferencyjny pomiar grubości składowej lipidowej i obrazowanie gruczołów Meiboma [4].
Leki a ZSO
Mechanizm działania leków na te części układu wydzielniczego, które są odpowiedzialne za tworzenie filmu łzowego, jest zróżnicowany. Duża część spośród leków mających wpływ na wystąpienie objawów suchego oka wykazuje ogólnoustrojowe działanie cholinolityczne.
Leki te oddziałują na receptory muskarynowe sprzężone z białkiem G gruczołów łzowych oraz na spojówkowe komórki kubkowe, wydzielające składową mucynową. Prowadzi to do zmniejszenia wydzielania składowej wodnej i białkowej oraz obniżenia stabilności filmu łzowego [5].
Obecność receptorów cholinergicznych została także potwierdzona w gruczołach Meiboma, więc cholinolityki mogą także powodować zmniejszanie wydzielania składowej lipidowej [6].
Leki z tej grupy są inhibitorami receptorów gruczołów łzowych, dlatego tutaj – również ze względu na przewlekły charakter stosowania leków, jak w astmie lub przewlekłej obturacyjnej chorobie płuc – istnieje duże ryzyko wystąpienia ZSO.
Z drugiej strony leki wpływające na receptory adregeniczne (zarówno pobudzająco, jak i hamująco), w tym β-blokery i α-agoniści, wywołują zmiany w jakości i ilości filmu łzowego za pośrednictwem kinazy białkowej C i wewnątrzkomórkowego stężenia jonów wapnia [7, 8].
Niektóre powszechnie stosowane leki, takie jak kwas acetylosalicylowy, mogą powodować zaostrzenie objawów suchego oka z powodu wytrącania się ich osadów w filmie łzowym i mechanicznego podrażniania powierzchni gałki ocznej [9].
Natomiast nadmiar kwasu retinowego, którego metabolity są wydzielane przez gruczoły łzowe, przyczynia się do atrofii gruczołów Meiboma, prowadząc do zmniejszenia ilości składowej lipidowej [10].
| Przykłady grup leków, które mogą powodować ZSO [28]: |
|
Kobiety są bardziej narażone na występowanie ZSO niż mężczyźni [11] ze względu na gospodarkę hormonalną. Estrogen jest hormonem wpływającym na wydzielanie składowej wodnej filmu łzowego.
Przyjmowany wraz z tabletkami antykoncepcyjnymi lub w ramach hormonalnej terapii zastępczej może prowadzić do wystąpienia ZSO. Częstotliwość występowania ZSO jest o 69% większa u kobiet poddających się hormonalnej terapii zastępczej niż u kobiet z grupy kontrolnej [12].
Leki przeciwhistaminowe, podobnie jak cholinolityki, również bezpośrednio wpływają na działanie gruczołów łzowych i komórek kubkowych – zmniejszają wydzielanie składowej wodnej i mucynowej filmu łzowego, obniżają jego stabilność i skracają czas przerwania [14].
Efektem ubocznym stosowania trój- i czterocyklicznych leków antydepresyjnych, hamujących wychwyt zwrotny serotoniny, jest również zmniejszenie wydzielania składowej wodnej przez gruczoły łzowe. ZSO może dotykać nawet 70% pacjentów przyjmujących leki antydepresyjne, a częstość występowania zależy w tym przypadku także od długości czasu trwania leczenia i wieku pacjenta [15].
Kolejną grupą leków zmniejszającą wydzielanie składowej wodnej filmu łzowego są β-blokery, stosowane w leczeniu nadciśnienia tętniczego, nadczynności tarczycy i jaskry. Powodują one zmniejszenie wydzielania lizozymu, immunoglobuliny A i składowej wodnej, prowadząc do objawów suchego oka.
Niektóre badania wykazały, że β-blokery zmniejszają czucie rogówkowe, co mogłoby zwiększać odstęp czasu między mrugnięciami, jednak doniesienia w tym zakresie są sprzeczne [16]. W przypadku β-blokerów jako kropli do oczu w leczeniu jaskry istotna jest konieczność ich długotrwałego stosowania, zazwyczaj do końca życia.
Obecne w kroplach konserwanty mogą również prowadzić do istotnego pogorszenia jakości filmu łzowego (zmniejszenie wydzielania wykrywane testem Schrimera i skrócenie czasu przerwania filmu łzowego), a w efekcie podrażnień i ubytków w nabłonku rogówki i spojówki (wybarwianie ubytków fluoresceiną w badaniu oftalmoskopowym) [17].
Konserwanty w kroplach do oczu a ZSO
Wpływ konserwantów zawartych w kroplach do oczu na ZSO wymaga osobnego omówienia. Konserwant najczęściej stosowany w kroplach do oczu, chlorek benzalkoniowy (BAK), ma udokumentowany wpływ na powstawanie uszkodzeń w obrębie powierzchni gałki ocznej, a jego działanie ma tendencję do nasilania się z biegiem czasu [18].
W badaniu przeprowadzonym na 9658 pacjentach chorujących na jaskrę przeanalizowano wpływ obecności konserwantów w kroplach do oczu na występowanie objawów ZSO. Wśród uczestników stosujących krople z konserwantami uczucie pieczenia (48%), ciała obcego (42%) lub suchości oka (35%) oraz ubytki nabłonka rogówki (26%) występowały znacznie częściej niż wśród uczestników stosujących krople bez konserwantów, odpowiednio: 20, 15, 16 i 9% [19].
BAK wykazuje działanie toksyczne i prozapalne, a także jest środkiem powierzchniowo czynnym, zmniejszającym stabilność warstwy lipidowej filmu łzowego. Komórki kubkowe wydzielające składową mucynową są wrażliwe na jego działanie.
Potwierdzono zmniejszenie gęstości komórek kubkowych po ich ekspozycji na BAK, a także zmniejszenie ilości mucyn na komórkach nabłonka rogówki i twardówki [20, 21]. BAK wykazał również działanie cytotoksyczne względem zakończeń nerwu trójdzielnego, unerwiającego rogówkę [22].
ZSO a chirurgia refrakcyjna i zaćma
Prawidłowe nawilżenie i odpowiednia kondycja powierzchni rogówki ma duże znaczenie u pacjentów zgłaszających się do kliniki okulistycznej na wizytę kwalifikacyjną do operacji zaćmy lub refrakcyjnej wymiany soczewki, lub też laserowej korekcji wady wzroku.
Pierwsze dwa z wymienionych zabiegów polegają na usunięciu naturalnej soczewki i wszczepieniu implantu o odpowiedniej mocy (wyrażonej w dioptriach). U pacjenta musi zostać wykonane między innymi badanie keratometrii, czyli krzywizny i mocy optycznej rogówki, niezbędne do prawidłowego wyznaczenia mocy implantu.
ZSO prowadzi do błędów w pomiarze i zafałszowania wyników keratometrii, a w konsekwencji do nieoptymalnego doboru mocy implantu i pozostawienia resztkowej wady wzroku po operacji [23].
Laserowa korekcja wady wzroku polega na odpowiedniej modyfikacji kształtu rogówki przez usunięcie części tkanki w taki sposób, aby stała się ona bardziej płaska (w korekcji krótkowzroczności) lub stroma (w nadwzroczności).
Chociaż ZSO nie stanowi bezwzględnego przeciwwskazania do rogówkowej chirurgii refrakcyjnej, to suche oko przyczynia się do wydłużenia czasu gojenia i rekonwalescencji po zabiegu.
Jest to spowodowane uszkodzeniem zakończeń nerwowych w rogówce i zmniejszonym czuciem rogówkowym, prowadzącym do zmniejszenia wydzielania łez i wydłużenia odstępu między mrugnięciami [24].
Czynnikiem wpływającym na zwiększone ryzyko wystąpienia ZSO po chirurgii refrakcyjnej jest zmieniony kształt rogówki i związane z nim nieprawidłowe rozłożenie filmu łzowego na powierzchni gałki ocznej, a także zmiana składu łez spowodowana uszkodzeniem komórek kubkowych [25, 26].
Podsumowanie
Pozornie ZSO wydaje się być zagadnieniem błahym, jednak może przyczyniać się do znacznego obniżenia komfortu życia osób nim dotkniętych. Największym ryzykiem związanym z ZSO jest syndrom nawracających erozji rogówki, czyli przerwanie ciągłości nabłonka rogówki, wywołujące silne dolegliwości bólowe i światłowstręt, uniemożliwiające codzienne funkcjonowanie [27].
ZSO może nieść długofalowe konsekwencje w przypadku pacjentów kwalifikowanych do operacji zaćmy lub refrakcyjnej wymiany soczewki, jeśli wpłynie on na wynik pomiaru krzywizny rogówki, a w konsekwencji na wyznaczoną moc implantu i refrakcję pooperacyjną.
Źródła:
-
-
-
-
-
-
-
- Friedman N.J.: Impact of dry eye disease and treatment on quality of life. Current Opinion in Ophthalmology. 2010. Vol. 21, No. 4, 310-316.
- Craig J.P., Nichols K.K., Nichols J.J., Caffery B., Dua H.S., Akpek E.K., et al. TFOS DEWS II Definition and Classification Report. The Ocular Surface. 2017. Vol. 15, No. 3, 276-283.
- Nelson J.D., Craig J.P., Akpek E.K., Azar D.T., Belmonte C., Bron A.J., Clayton J.A., Dogru M., Dua H.S., Foulks G.N., Gomes J.A.P., Hammitt K.M., Holopainen J., Jones L., Joo C.K., Liu Z., Nichols J.J., Nichols K.K., Novack G.D., Sangwan V., Stapleton F., Tomlinson A., Tsubota K., Willcox M.D.P., Wolffsohn J.S., Sullivan D.A.: TFOS DEWS II Introduction. . The Ocular Surface. 2017. Vol. 15, No. 3, 269-275.
- Wolffsohn J.S., Arita R., Chalmers R., Djalilian A., Dogru M., Dumbleton K., Gupta P.K., Karpecki P., Lazreg S., Pult H., Sullivan B.D., Tomlinson A., Tong L., Villani E., Yoon K.C., Jones L., Craig J.P.: TFOS DEWS II Diagnostic Methodology report. The Ocular Surface. 2017. Vol. 15, No. 3, 539-574.
- Apostol S., Filip M., Dragne C., Filip A.: Dry eye syndrome. Etiological and therapeutic aspects. Oftalmologia. 2003. Vol. 9, No. 4, 28-31.
- Kam W.R., Sullivan D.A.: Neurotransmitter influence on human meibomian gland epithelial cells. Investigative Ophthalmology & Visual Science. 2011. Vol. 52, No. 12, 8543-8548.
- Mackie I.A., Seal D.V., Pescod J.M.: Beta-adrenergic receptor blocking drugs: tear lysozyme and immunological screening for adverse reaction. British Journal of Ophthalmology. 1977. Vol. 61, No. 5, 354-359.
- Jaanus S.D.: Ocular side effects of selected systemic drugs. Optometry Clinics: the Official Publication of the Prentice Society. 1992. Vol. 2, No. 4, 73-96.
- Klein B.E., Howard K.P., Gangnon R.E., Dreyer J.O., Lee K.E., Klein R.: Long-term use of aspirin and age-related macular degeneration. JAMA. 2012. Vol. 308, No. 23, 2469-2478.
- Mathers W.D., Shields W.J., Sachdev M.S., Petroll W.M., Jester J.V.: Meibomian gland morphology and tear osmolarity: changes with Accutane therapy. Cornea 1991. Vol. 10, No. 4, 286-290.
- Gomes J.A.P., Azar D.T., Baudouin C., Efron N., Hirayama M., Horwath-Winter J., Kim T., Mehta J.S., Messmer E.M., Pepose J.S., Sangwan V.S., Weiner A.L., Wilson S.E., Wolffsohn J.S.: TFOS DEWS II iatrogenic report. The Ocular Surface. 2017. Vol. 15, No. 3, 511-538.
- Schaumberg D.A., Buring J.E., Sullivan D.A., Dana M.R.: Hormone replacement therapy and dry eye syndrome. JAMA. 2001. Vol. 286, No. 17, 2114-2119.
- Nietgen G.W., Schmidt J., Hesse L., Hönemann C.W., Durieux M.E.: Muscarinic receptor functioning and distribution in the eye: molecular basis and implications for clinical diagnosis and therapy. Eye. 1999. Vol. 13, 285-300.
- Ousler G.W. 3rd., Workman D.A., Torkildsen G.L.: An open-label, investigator-masked, crossover study of the ocular drying effects of two antihistamines, topical epinastine and systemic loratadine, in adult volunteers with seasonal allergic conjunctivitis. Clinical Therapeutics. 2007. Vol. 29, No. 4, 611-616.
- Mrugacz M., Ostrowska L., Łazarczyk-Kirejczyk J., et al.: Dry eye disease in patients treated with antidepressants. Klinika Oczna. 2013. Tom 115, nr 2, 111-114.
- Martin X.Y., Safran A.B.: Corneal hypoesthesia. Survey of Ophthalmology. 1988. Vol. 33, No. 1, 28-40.
- Iester M., Telani S., Frezzotti P., Motolese I., Figus M., Fogagnolo P., Perdicchi A.: Beta-Blocker Study Group. Ocular surface changes in glaucomatous patients treated with and without preservatives beta-blockers. Journal of Ocular Pharmacology and Therapeutics. 2014. Vol. 30, No. 6, 476-481.
- Broadway D.C., Grierson I., O’Brien C., Hitchings R.A.: Adverse effects of topical antiglaucoma medication. II. The outcome of filtration surgery. Archives of Ophthalmology. 1994. Vol. 112, No. 11, 1446-1454.
- Jaenen N., Baudouin C., Pouliquen P., Manni G., Figueiredo A., Zeyen T.: Ocular symptoms and signs with preserved and preservative-free glaucoma medications. European Journal of Ophthalmology. 2007. Vol. 17, No. 3, 341-349.
- Chung S.H., Lee S.K., Cristol S.M., Lee E.S., Lee D.W., Seo K.Y., et al.: Impact of short term exposure of commercial eyedrops preserved with benzalkonium chloride on precorneal mucin. Molecular Vision. 2006. Vol. 12, 415-421.
- Kahook M.Y., Noecker R.: Quantitative analysis of conjunctival goblet cells after chronic application of topical drops. Advances in Therapy. 2008. Vol. 25, No. 8, 743e51.
- Sarkar J., Chaudhary S., Namavari A., Ozturk O., Chang J.H., Yco L., et al.: Corneal neurotoxicity due to topical benzalkonium chloride. Investigative Ophthalmology & Visual Science. 2012. Vol. 53, No. 4, 1792-1802.
- Epitropoulos A.T., Matossian C., Berdy G.J., Malhotra R.P., Potvin R.: Effect of tear osmolarity on repeatability of keratometry for cataract surgery planning. Journal of Cataract & Refractive Surgery. 2015. Vol. 41, No. 8, 1672-1677.
- Maychuk D.Y.: Dry Eye Prevalence Study Group. Prevalence and severity of dry eye in candidates for laser in situ keratomileusis for myopia in Russia. Journal of Cataract & Refractive Surgery. 2016. Vol. 42, No. 3, 427-434.
- Toda I., Asano-Kato N., Hori-Komai Y., Tsubota K.: Laser-Assisted In Situ Keratomileusis for Patients With Dry Eye. Archives of ophthalmology. 2002. Vol. 120, No. 8, 1024-1028.
- Konomi K., Chen L.L., Tarko R.S., Scally A., Schaumberg D.A., Azar D., Dartt D.A.: Preoperative characteristics and a potential mechanism of chronic dry eye after LASIK. Investigative Ophthalmology & Visual Science. 2008. Vol. 49, No. 1, 168-174.
- Miller D.D., Hasan S.A., Simmons N.L., Stewart M.W.: Recurrent corneal erosion: a comprehensive review. Clinical Ophthalmology. 2019. Vol. 13, 325-335.
- Roberts D.: The managment of dry eye. Sage Journals. 2015. Vol. 8, No. 7, 412-417.
- Szczęsna D.: Badania i ocena kinetyki filmu łzowego za pomocą interferometrii. https://www.dbc.wroc.pl (stan z dn. 15.01.2021 r.).
-
-
-
-
-
-


