Bezpieczeństwo stosowania leków podczas karmienia piersią
Udostępnij

Kobiety karmiące piersią sięgają po leki częściej niż kobiety w ciąży. W badaniach prowadzonych w Ameryce przez Stulz i współpracowników wykazano, że ponad 96% kobiet podczas laktacji przyjmowało jeden lub więcej leków, z czego większość preparatów stanowiła leki bez recepty. Odnotowano także, że kobiety te nie posiadały wystarczających informacji o bezpieczeństwie stosownych leków, a część z tych leków mogła prowadzić do wystąpienia potencjalnych działań niepożądanych u karmionych dzieci [1]. Badania przeprowadzone w Kanadzie wykazały, że 80% kobiet w pierwszym roku po porodzie miało przepisany jeden lub więcej leków na receptę, a 61% tych kobiet karmiła dzieci przez pierwsze sześć miesięcy [2].
Konieczność przyjmowania leków w okresie laktacji może przyczynić się także do przedwczesnego zaprzestania karmienia [3], pomimo tego, że większości leków uważa się za kompatybilne z laktacją [4, 5]. Karmienie piersią posiada wiele zalet, jest rekomendowane przez wiele towarzystw naukowych, dlatego nie można pozwolić by z braku wiedzy lub niewystarczającego dostępu do informacji dochodziło do przerwania laktacji [3, 5, 6]. W proces edukacji oraz poradnictwa powinni zaangażować się lekarze, farmaceuci, położne oraz doradcy laktacyjni, tworząc zespół terapeutyczny wspierający kobiety karmiące piersią [7, 8, 9].
W każdym przypadku członkowie zespołu terapeutycznego powinni rozważyć indywidualne bezpieczeństwo stosowania leku przez kobiety karmiące. W ocenie stosunku korzyści do ryzyka należy wziąć pod uwagę następujące aspekty:
- Czy lek jest potrzebny matce?
- Jakie właściwości fizykochemiczne, farmakodynamiczne i farmakokinetyczne posiada zlecony lek? W jakiej dawce i postaci farmaceutycznej zostanie zaordynowany?
- Jaki wpływ będzie wykazywać rekomendowany lek na produkcję mleka?
- W jakim stopniu lek przeniknie do pokarmu matki? (ilość wydzielonego leku do pokarmu)
- Jaka będzie biodostępność leku u niemowlęcia karmionego piersią?
- Jakie ryzyko działań niepożądanych u dziecka niesie za sobą podanie tego leku?
- Jak długo lek będzie stosowany?
- W jakim wieku jest dziecko?
- Jaki sposób karmienia niemowlęcia jest praktykowany?
- Czy jest konieczność zakończenia laktacji lub alternatywa terapeutyczna pozwalająca na utrzymanie i kontynuowanie laktacji?
Wydzielanie leków do pokarmu zachodzi w większości przypadków na drodze dyfuzji biernej oraz zdecydowanie rzadziej przy udziale transportu aktywnego opartego na nośnikach. Dyfuzja bierna leku do mleka zależy od stężenia leku we krwi matki oraz od właściwości fizykochemicznych leku. Stężenie leku w pokarmie jest proporcjonalne do stężenia leku we krwi matki, co może wynikać z zastosowanej wysokiej dawki leku lub procesów związanych z farmakokinetyką leku w organizmie matki [2]. Właściwości fizykochemiczne cząsteczki leku mają wpływ na przenikanie leku do pokarmu matki. Do pokarmu wydzielane są leki lipofilne o małej masie cząsteczkowej (poniżej 500 Da), o niskim stopniu wiązania z białkami, a także o charakterze słabych zasad [2, 3, 10].
Na podstawie informacji o dawce leku zażywanej przez matkę można określić względną dawkę przyjmowaną przez karmione dziecko, RID (ang. relative infant dosage). Za bezpieczne dla karmionego dziecka uznaje się leki o wartości RID mniejszej niż 10% (Tabela 1). Leki, których RID wynosi więcej niż 25% nie są zalecane do stosowania w czasie laktacji [2, 3, 11].
Wskaźnik M/P (ang. Milk/Plasma Ratio) charakteryzuje stosunek stężenia leku w mleku matki (M) do stężenia w surowicy matki (P) i pozwala na oszacowanie miejsca, w którym lek osiągnie wyższe stężenie. Leki o współczynniku M/P mniejszym od 1 są uznawane za bezpieczne, ponieważ są wydalane szybko z organizmu i/lub mają charakter hydrofilny i/lub charakter kwaśny, przez co nawet przy wielokrotnym podaniu takiego leku prawdopodobieństwo oznaczenia jego stężeń we krwi dziecka jest niskie. Leki o współczynniku M/P równym lub wyższym 1 charakteryzują się mniejszym profilem bezpieczeństwa. Są to leki lipofilne i/lub o charakterze zasadowym i/lub wolno eliminowane z organizmu matki, dlatego istnieje ryzyko, że lek osiągnie wysokie stężenia we krwi dziecka [2, 3, 11, 12].
Zalecenia dla członków zespołu terapeutycznego związane z ordynowaniem leków dla kobiet karmiących (opracowanie własne na podstawie 3, 5, 10, 11, 13, 14):
1. Należy opracować pisemne indywidualne zalecenia w oparciu o wiarygodne oraz aktualne źródła informacji. Zaleca się przeanalizować stosowane do tej pory preparaty, potwierdzić zasadność ich przyjmowania oraz ocenić bezpieczeństwo wprowadzenia nowego leku. Zadaniem członków zespołu terapeutycznego jest także zwiększenie świadomości kobiet związanej z bezpieczeństwem stosowaniem leków bez recepty oraz działalność edukacyjna ograniczająca ich stosowanie.
2. Należy promować karmienie piersią, nawet w przypadku konieczności czasowego przerwania lub zawieszenia laktacji podczas farmakoterapii. Warto zwrócić uwagę na aspekty techniczne związane z czynnością jaką jest karmienie piersią (sposób przystawienia dziecka, technika ssania, pobudzanie laktacji przez odciąganie pokarmu).
3. Niezbędna jest skuteczna komunikacja pomiędzy członkami zespołu terapeutycznego a pacjentką, szczególnie w przypadku, gdy informacje o bezpieczeństwie stosowania danego leku są nieznane lub rozbieżne. Należy poinformować pacjentkę o korzyści oraz ryzyku związanym z wprowadzeniem leku i pozwolić na podjęcie przez nią decyzji.
4. Przy wyborze leku powinno uwzględniać się jego dawkę, właściwości fizykochemiczne, losy leku w ustroju matki, drogę podania oraz postać leku
- Zaleca się stosować leki o znanym profilu działania w stosunku do nowych wprowadzonych od niedawna na rynek
- Należy stosować najniższą skuteczną terapeutycznie dawkę leku przez możliwie jak najkrótszy czas.
- Jeżeli jest taka możliwość, to zaleca się stosować leki o niskiej biodostępności, nie ulegające wchłanianiu w przewodzie pokarmowym (np. wziewnie) lub stosować leki o działaniu miejscowym.
- W przypadku leków działających systemowo zaleca się ordynować leki o krótkim okresie biologicznego półtrwania, a unikać leków o modyfikowanym uwalnianiu.
- Preferowane są leki o wysokim stopniu wiązania z białkami (powyżej 90%) oraz o niskim współczynniku RID (mniej niż 10%), a także o niskim współczynniku M/P (mniej niż 1).Przy wyborze leku powinno uwzględniać się jego dawkę, właściwości fizykochemiczne, losy leku w ustroju matki, drogę podania oraz postać leku
5. Przy ordynowaniu leków należy zwrócić uwagę na wiek dziecka. Na częste manifestacje działań niepożądanych leków narażone są najbardziej dzieci urodzone przedwcześnie, co wynika ze zmniejszonej aktywności metabolicznej wątroby oraz niesprawnej czynności wydzielniczej nerek. Umiarkowane ryzyko występowania skutków ubocznych leków stosowanych przez matkę dotyczy niemowląt pomiędzy drugim tygodniem a szóstym miesiącem życia. Niskie ryzyko pojawienia się działań niepożądanych opisywano u dzieci karmionych piersią pomiędzy szóstym a osiemnastym miesiącem życia.
6. Należy przeanalizować sposób i częstotliwość karmienia piersią, by zaplanować odpowiednie przedziały dawkowania leku w oparciu o jego właściwości fizykochemiczne i farmakologiczne.
- unikać karmienia w czasie, gdy lek osiąga najwyższe stężenie we krwi matki,
- przyjmować lek bezpośrednio po karmieniu
7. Zaleca się monitorować efekty stosowanego przez matkę leku u dziecka; wskazać pacjentce potencjalne działania uboczne, obserwować działania niepożądane czy niepokojące objawy u dziecka
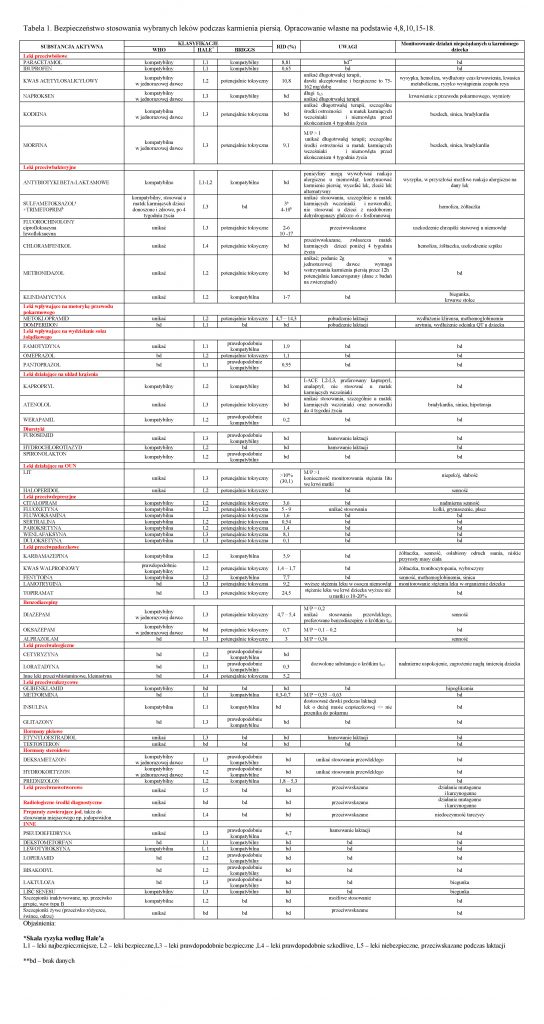
Przykładowe informacje o bezpieczeństwie stosowania wybranych leków w trakcie karmienia piersią umieszczono w Tabeli nr 1, która znajduje się na końcu tego materiału.
Wiarygodne i aktualne źródła informacji
Przekazywane informacje dla kobiet karmiących na temat bezpieczeństwa stosowania leków powinny opierać się na wiarygodnych i aktualnych źródłach wiedzy. Główne źródło wiedzy powinna stanowić charakterystyka produktu leczniczego (ChPL). Nie zawsze jednak dostępne są w niej wystarczające informacje o bezpieczeństwie stosowania leku podczas karmienia piersią, dlatego należy szukać danych w innych źródłach. Obecnie dostępnych jest wiele klasyfikacji oraz baz danych opisujących właściwości konkretnego leku, zebrano je w Tabeli nr 2.
Tabela 2. Zalecane źródła informacji związane ze stosowaniem leków w czasie laktacji. (Opracowanie własne).
| Zalecane źródła informacji na temat leków stosowanych podczas laktacji | |
| Rekomendacje Światowej Organizacji Zdrowia (WHO 2002) | Breastfeeding And Maternal Medication Recommendations for Drugs in the Eleventh WHO Model List of Essential Drugs
https://www.who.int/maternal_child_adolescent/documents/55732/en/
|
| Raport Amerykańskiej Akademii Pediatrii
(AAP 2013) |
The Transfer of Drugs and Therapeutics Into Human Breast Milk: An Update on Selected Topics www.pediatrics.org/cgi/doi/10.1542/peds.2013-1985
|
| Agencja Żywności i Leków (FDA 2014) | Content and Format of Labeling for Human Prescription Drug and Biological Products; Requirements for Pregnancy and Lactation Labeling
http://federalregister.gov/a/2014-28241
|
| Skala ryzyka wg Hale’a | „Hale’s Medications & Mothers’ Milk”
Springer Publishing Company 2019 |
| Briggs G.G.
|
“A Reference Guide To Fetal And Neonatal Risk Drugs in Pregnancy and Lactation”
Wolters Kluwer Health 2015 |
| LactMed | https://toxnet.nlm.nih.gov/newtoxnet/lactmed.htm
|
| e-lactancia | http://www.e-lactancia.org/
|
| Laktacyjny Leksykon Leków | http://www.kobiety.med.pl/leki/search.php
|
Podsumowanie
Ograniczona możliwość stosowania leków przez kobiety karmiące wynika z braku danych na temat nowych leków oraz preparatów roślinnych, a nie z powodu wywoływanych przez nich skutków ubocznych. Brak danych wynika z regulacji prawnych, ponieważ kobiety w ciąży oraz karmiące nie mogą brać udziału w badanach klinicznych, a wyników z badań prowadzonych na zwierzętach nie można ekstrapolować na ludzi. Poznanie działań niepożądanych leków stosowanych podczas laktacji, czy to w wyniku badań farmakokinetycznych czy obserwacyjnych, pozwala na zarządzanie ryzykiem, wdrożenie alternatywnych rozwiązań oraz monitorowanie wpływu i skutków wprowadzonych do terapii matki leków.
W zdecydowanej większości przypadków leki stosowane przez matki karmiące mają bezpieczny profil działania a przez to nie ma konieczności przerywania laktacji podczas ich zażywania. Jednak ograniczony dostęp do personelu fachowego, korzystanie z porad umieszczonych na forach internetowych czy opieranie się na rekomendacjach członków rodziny przyczynia się niestety do czasowego wstrzymania lub zakończenia karmienia piersią. Należy więc dołożyć wszelkich starań, by farmakoterapia kobiet karmiących była bezpieczna dla nich oraz ich dzieci oraz by zmniejszyć ryzyko przerwania laktacji z powodu zaordynowanej terapii.
Dostęp do wiarygodnych i aktualnych baz danych nie jest trudny. Analiza informacji powinna być rzetelna oraz opierać się na medycynie opartej na dowodach. Dostępne w bazach danych informacje nie są zawsze jednoznaczne i spójne, co powoduje, że konieczne jest indywidualne podejście do każdego przypadku klinicznego oraz współpraca pomiędzy członkami zespołu terapeutycznego.
Autorki:
dr n. farm. Magdalena Olejniczak-Rabinek,
Apteka Szpitalna, Szpital Kliniczny im. Heliodora Święcickiego Uniwersytetu Medycznego im. Karola Marcinkowskiego w Poznaniu
dr n. med. Agata Kasprzyk
Instytut Hematologii i Transfuzji, Warszawa
Źródła:
-
-
- Stultz E.E., Stokes J.L., Shaffer M.L., Paul I.M., Berlin C.M.: Extent of Medication Use in Breastfeeding Women, Breastfeeding Medicine 2007, 2(3): 145-151
- Verstegen R. H.J., Ito S.: Drugs in lactation, J. Obstet. Res. 2019 doi:10.1111/jog.13899 [stan na 13.07.2020]
- Anderson P.O.: Drug in Lactation, Pharm Res 2018, 35-45 https://doi.org/10.1007/s11095-017-2287-z [stan na 15.07.2020]
- Sachs H.C. and Committee On Drugs: The Transfer of Drugs and Therapeutics Into Human Breast Milk: An Update on Selected Topics, Pediatrics 2013;132;e796, www.pediatrics.org/cgi/doi/10.1542/peds.2013-1985 doi:10.1542/peds.2013-1985 [stan na 13.07.2020]
- Hotham N., Hotham E., Drugs in breastfeeding, Aust Prescr 2015;38:156–9
- Heitmann K., Schjott J.: SafeMotherMedicine: Aiming to Increase Women’s Empowerment in Use of Medications During Pregnancy and Breastfeeding, Maternal and Child Health Journal https://doi.org/10.1007/s10995-020-02903-9 [stan na 14.07.2020]
- McClatchey A.K., Shield A., Cheong L.C., Ferguson S., Cooper G.M., Kyle G.J.: Why does the need for medication become a barrier to breastfeeding? A narrative review, Women Birth 2018 Oct;31(5):362-366. doi: 10.1016/j.wombi.2017.12.004. Epub 2017 Dec 16. [stan na 16.07.2020]
- Hussainy S.Y., Dermele N.: Knowledge, attitudes and practices of health professionals and women towards medication use in breastfeeding: A review; International Breastfeeding Journal 2011, 6:11 http://www.internationalbreastfeedingjournal.com/content/6/1/11 [stan na 17.07.2020]
- De Ponti M., Stewart K., Lisa H. Amir L.H., Hussainy S.Y.: Medicine use and safety while breastfeeding: investigating the perspectives of community pharmacists in Australia, Australian Journal of Primary Health, 2015, 21, 46–57; http://dx.doi.org/10.1071/PY13012 [stan na 15.07.2020]
- Rowe H., Baker T., Hale T.W.: Maternal Medication, Drug Use, and Breastfeeding, Pediatr Clin N Am 60 (2013) 275–294, http://dx.doi.org/10.1016/j.pcl.2012.10.009 [stan na 17.07.2020]
- Kowol-Trela K., Mijas J., Nehring-Gugulska M.: Czy mleko matki zawsze jest bezpieczne dla dziecka? Farmakoterapia matki karmiącej. Post N Med 2017; XXX(09): 500-503
- Von Mandach U.: Ciąża i laktacja; Jaehde U., Radziwill R., Kloft C., red. Wiela – Hojeńska A i inni: Farmacja Kliniczna, MedPharm 2017, 424-426
- Bertino E., Varalda A., Di Nicola P., Coscia A., Occhi L., Vagliano L., Soldi A., Perathoner C., Drugs and breastfeeding: instructions for use, The Journal of Maternal-Fetal and Neonatal Medicine, 2012; 25(S4): 78–80
- Kamińska E., Lauterbach R.: Stosowanie leków a karmienie piersią, Pediatria po Dyplomie 2011, 15 (6): 77-85
- Kronenfeld N., Berlin M., Shaniv D., Berkovitch M: Use of Psychotropic Medications in Breastfeeding Women, Birth Defects Research 2017, 109: 957–997
- Breastfeeding And Maternal Medication Recommendations for Drugs in the Eleventh WHO Model List of Essential Drugs, World Health Organization 2002
- Briggs G.G.: A Reference Guide To Fetal And Neonatal Risk Drugs in Pregnancy and Lactation, Tenth Edition, Wolters Kluwer Health 2015
- Powrie R.O, Greene M.F., Camann W.: de Swiet’s Medical Disorders in Obstetric Practice, 5th Edition, Blackwell Publishing 2010, Appendix: Medications and their relative risk to breastfeeding infants p.759-769
-


